GynTect®
In-vitro-Diagnostik von Gebärmutterhalskrebs
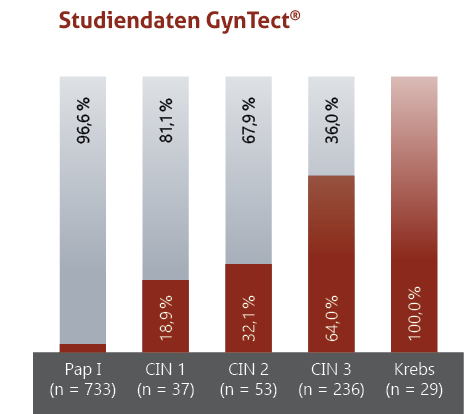
GynTect® wird in der In-vitro-Diagnostik von Gebärmutterhalskrebs eingesetzt. Der molekularbiologische Test basiert auf der Detektion von DNA-Methylierung in humanen Genregionen. Der Nachweis der GynTect®-Marker erfolgt durch eine Echtzeit-Polymerase-Kettenreaktion (PCR).